Im letzten Abschnitt haben wir Metall-Nanopartikeln und ihre Eigenschaften kennengelernt. Jetzt wollen wir uns eine andere Kategorie von farbigen Nanopartikeln ansehen, sogenannte „Quantenpunkte“.
Quantenpunkte sind sehr kleine Teilchen mit einer Größe von wenigen Nanometern und sie bestehen aus Materialien, die „Halbleiter“ genannt werden. Dazu gehören zum Beispiel Indiumphosphid oder Zinkselenid. Das besondere an diesen Teilchen ist, dass sie, anders als die oben gezeigten plasmonischen Teilchen, erst dann eine Farbe zeigen, wenn man sie mit hochenergetischem Licht einer kleineren Wellenlänge, wie ultraviolettem Licht, bestrahlt (siehe dazu auch Grundlagen: Gibt es noch anderes Licht?).

Warum ist das so?
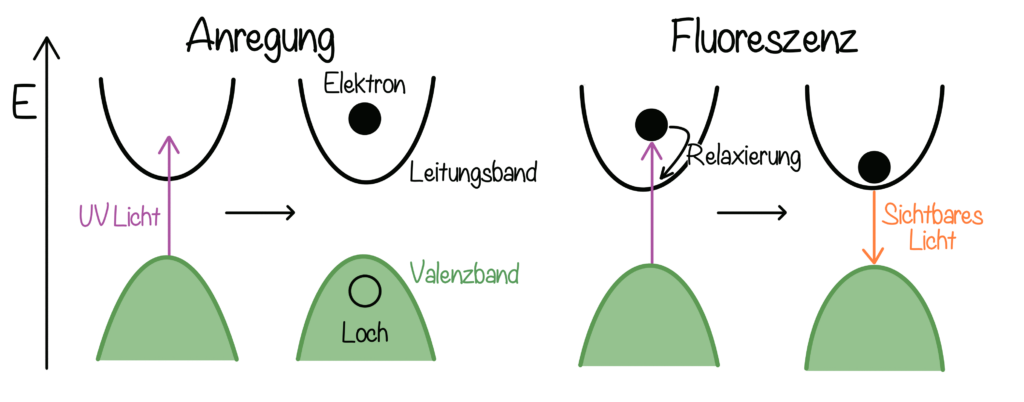
Dafür müssen wir uns die elektronische Struktur der Halbleiterpartikeln anschauen. Du kannst dir vorstellen, dass Halbleitermaterialien auf elektronischer Ebene zwei Energieebenen besitzen, auf denen sich die negativ geladenen Elektronen aufhalten können: das untere Valenz- und das obere Leitungsband. Man kann sich dies wie zwei Stockwerke in einem Gebäude vorstellen. Die beiden Bänder, in denen die Elektronen sich aufhalten können, sind voneinander getrennt. Man muss einem Elektron im unteren Band erst Energie zufügen, damit es in das Band ‚im höheren Stockwerk‘ wandern kann. Wenn nun eine energiereiche Lichtwelle (typischerweise mit kleineren Wellenlängen als sichtbares Licht, also im ultravioletten Bereich) auf die Quantenpunkte trifft, stellt die Lichtwelle genau diese Energie zur Verfügung. Die Elektronen aus der unteren Ebene werden wie mit einem Aufzug in die obere Ebene gebracht. Man sagt nun, diese Elektronen sind „energetisch angeregt“. Sie besitzen nun eine höhere Energie. Doch das bleibt nicht lange so, denn das Elektron möchte so wenig Energie wie möglich besitzen. Deshalb wird es den energetisch niedrigsten Punkt im oberen ‚Geschoss‘ einnehmen, man spricht dabei von „Relaxierung“, und anschließend wieder zurück ins ‚Erdgeschoss‘, den Grundzustand, übergehen. Bei diesem Übergang gibt das Elektron die zuvor zugefügte Energie wieder ab, die als Lichtwelle ausgestrahlt wird. Dieser Prozess heißt „Fluoreszenz“. Die Energie der ausgesandten Lichtwelle hängt davon ab, wie groß der Energieunterschied zwischen den ‚Stockwerken‘ oder Bändern ist und definiert damit auch die Farbe der ausgesandten Lichtwelle.
Den Energieunterschied zwischen den Bändern kann man durch die Größe der Partikeln einstellen: größere Quantenpunkte zeigen eine rote Farbe und kleinere Quantenpunkte zeigen eine blaue Farbe. Die Größen dazwischen ergeben die übrigen Farben des Regenbogens.

Anwendungsbeispiel

Quantenpunkte werden bereits in großen Mengen in der Industrie produziert. Im Jahr 2023 wurde sogar der Nobelpreis für Chemie für die Entdeckung der Quantenpunkte verliehen. Vielleicht bist du ja auch schon einmal über das Wort „Quantenpunkt“oder „Quantum“ gestolpert? Fällt dir ein wo? Dann schreibe es in die Kommentare.

Ist dir ein Beispiel eingefallen? Quantenpunkte sind dafür bekannt, dass sie in modernen QLED (oder Quantum LED)-Fernsehern zum Einsatz kommen, um eine bessere Bildqualität zu erreichen. Das kommt daher, dass die Farben der Quantenpunkte sehr definiert – also scharf sind. So lassen sich besser verschiedene Farben zusammenmischen, weil man gezielter einzelne Zäpfchen in unserem Auge ansprechen kann (Hier geht es zu dem Exkurs, wie das menschliche Auge Licht wahrnimmt). So entsteht ein farbechteres Bild.
